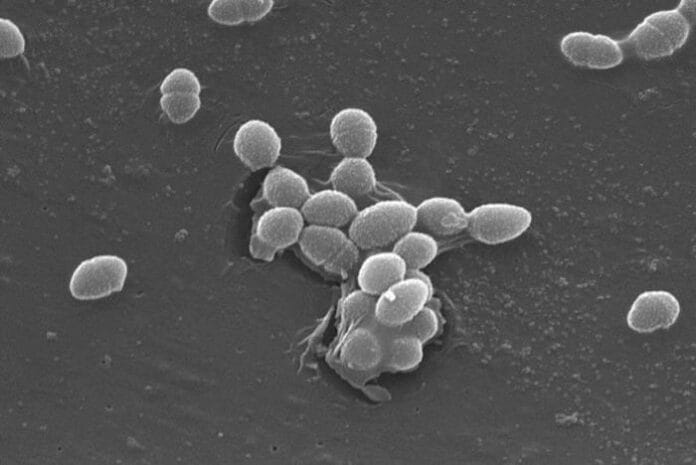
La bacteria Enterococcus faecalis logra evadir las defensas del organismo y favorecer infecciones persistentes y complejas
Las infecciones crónicas de heridas, como las úlceras del pie diabético o las infecciones tras cirugía, siguen siendo uno de los grandes desafíos clínicos por su resistencia al tratamiento y su lenta curación. Ahora, un estudio internacional arroja nueva luz sobre este problema al identificar un mecanismo clave mediante el cual la bacteria Enterococcus faecalis logra evadir las defensas del organismo y favorecer infecciones persistentes y complejas.
La investigación, publicada en la revista Cell Host & Microbe, revela que esta bacteria utiliza el ácido láctico como arma para «silenciar» el sistema inmunitario en el lugar de la infección. Este hallazgo no solo ayuda a entender por qué algunas heridas no cicatrizan adecuadamente, sino que abre la puerta a nuevas estrategias terapéuticas más allá de los antibióticos.
Enterococcus faecalis es un microorganismo habitual en el intestino humano, donde normalmente no causa problemas. Sin embargo, en determinadas circunstancias —como en pacientes hospitalizados o inmunodeprimidos— puede convertirse en un patógeno oportunista responsable de infecciones graves, especialmente en heridas y dispositivos médicos.
Estas infecciones suelen ser además polimicrobianas, es decir, implican a varias especies bacterianas, lo que complica aún más su tratamiento. Tradicionalmente, esta dificultad se ha atribuido a factores como la resistencia a los antibióticos o la formación de biopelículas. Sin embargo, el nuevo estudio apunta a un mecanismo adicional: la manipulación directa de la respuesta inmunitaria del huésped.
El papel clave del ácido láctico
Los investigadores demostraron que E. faecalis libera grandes cantidades de ácido láctico en el entorno de la herida. Este compuesto, conocido por su papel en el metabolismo celular, tiene aquí una función muy distinta: acidificar el entorno y bloquear la activación de los macrófagos, células fundamentales del sistema inmunitario encargadas de detectar y eliminar patógenos.
El ácido láctico actúa a través de dos vías complementarias. Por un lado, entra en los macrófagos mediante el transportador MCT-1, alterando el equilibrio interno de la célula y reduciendo su pH. Por otro, activa un receptor en la superficie celular llamado GPR81. Ambas rutas convergen en un mismo efecto: la inhibición de la vía de señalización NF-κB, un elemento central en la respuesta inflamatoria.
Esta vía funciona normalmente como una «alarma» que activa genes relacionados con la inflamación y la defensa antimicrobiana. Sin embargo, al ser bloqueada por el ácido láctico, los macrófagos no llegan a activarse completamente, lo que impide que el sistema inmunitario responda de forma eficaz.
El estudio profundiza en los mecanismos moleculares implicados en este proceso. El ácido láctico interfiere con la fosforilación de proteínas clave como ERK y STAT3, lo que reduce los niveles de MyD88, un adaptador esencial para activar NF-κB. Paralelamente, la activación del receptor GPR81 induce cambios en el factor de transcripción YAP, lo que también contribuye a frenar la respuesta inflamatoria.
«Las infecciones crónicas de heridas a menudo fracasan no porque los antibióticos sean ineficaces, sino porque el sistema inmunitario está prácticamente desactivado en el lugar de la infección», explicó Ronni da Silva, primer autor del estudio. «E. faecalis inunda la herida con ácido láctico, reduce el pH y silencia la señal de alarma de los macrófagos».
Evidencia en modelos experimentales
Los hallazgos fueron validados en un modelo de heridas en ratones. Las cepas de E. faecalis incapaces de producir ácido láctico fueron eliminadas mucho más rápidamente por el sistema inmunitario, y las heridas mostraron una mayor actividad inflamatoria.
Además, en infecciones mixtas con la bacteria Escherichia coli, la supresión inmunitaria provocada por el ácido láctico permitió que esta segunda bacteria proliferara con mayor facilidad. Este resultado ayuda a explicar por qué las infecciones de heridas suelen volverse más complejas con el tiempo y más difíciles de tratar.
El descubrimiento tiene importantes implicaciones para el manejo de las infecciones crónicas. Actualmente, el tratamiento se basa principalmente en antibióticos, que no siempre son eficaces, especialmente en infecciones polimicrobianas o con bacterias resistentes.
Los autores sugieren que futuras estrategias terapéuticas podrían centrarse en restaurar la respuesta inmunitaria local. Entre las posibles aproximaciones se incluyen neutralizar la acidez de la herida o bloquear las vías de señalización activadas por el ácido láctico, como MCT-1 o GPR81.
También se plantea el uso de agentes inmunomoduladores. En el estudio, un activador de STAT3 logró reducir la carga bacteriana tanto en experimentos in vitro como en modelos animales, lo que refuerza la idea de que reactivar el sistema inmunitario podría ser clave para combatir estas infecciones.
«Al identificar cómo se desactiva la respuesta inmunitaria, podemos desarrollar tratamientos que no solo ataquen a las bacterias, sino que también ayuden al organismo a defenderse mejor», señaló Kimberly Kline, autora principal del trabajo.
Más allá de las heridas
Aunque el estudio se centra en infecciones cutáneas, los investigadores creen que este mecanismo podría estar presente en otros contextos clínicos, como infecciones urinarias asociadas a catéteres o infecciones del torrente sanguíneo.
Además, el papel del ácido láctico en la regulación inmunitaria no es exclusivo de las infecciones bacterianas. Procesos similares se han descrito en el microambiente tumoral, lo que sugiere que este metabolito podría desempeñar un papel más amplio en la modulación de la inmunidad.
Los investigadores planean ahora validar estos hallazgos en muestras humanas y explorar su aplicación en modelos preclínicos más avanzados. El objetivo final es trasladar este conocimiento a la práctica clínica y mejorar el tratamiento de las infecciones crónicas. En un contexto de creciente resistencia a los antibióticos, este tipo de enfoques, centrados en el sistema inmunitario, podrían marcar un cambio de paradigma en la lucha contra las infecciones persistentes.
En definitiva, el estudio no solo desvela una estrategia sorprendente de una bacteria común, sino que también abre nuevas vías para abordar uno de los problemas más complejos de la medicina actual: las heridas que no cicatrizan.